Расчет количества теплоты при плавлении и отвердевании. Расчет количества теплоты при теплопередаче, удельная теплоемкость вещества. Уравнение теплового баланса
Чашкина Татьяна Георгиевна
Место работы, должность:
Подгороднепокровская СОШ Оренбургского района, учитель физики
Оренбургская область
Характеристики урока (занятия)
Уровень образования:
Среднее (полное) общее образование
Целевая аудитория:
Учащийся (студент)
Целевая аудитория:
Учитель (преподаватель)
Класс(ы):
Предмет(ы):
Цель урока:
Тип урока:
Урок изучения и первичного закрепления новых знаний
Краткое описание:
1) Оргмомент. Целеполагание 2) Проверка домашнего задания 3) Изучение новой темы 4) Закрепление новой темы 5) Итоги урока 6) Домашнее задание
Урок №15
Тема урока: Расчёт количества теплоты при плавлении, кристаллизации
Цель: Дать понятия удельной теплоты плавления, вывести формулу Q = λ m, научить применять формулы Q = с m (tк -tн) и Q = λ m в решении задач, повторить понятие температуры плавления, удельной теплоёмкости
Ход урока: 1) Оргмомент. Целеполагание
2) Проверка домашнего задания
3) Изучение новой темы
4) Закрепление новой темы
5) Итоги урока
6) Домашнее задание
1.Здравствуйте ребята. Сегодня на уроке мы продолжим разговор о плавлении и кристаллизации. Для этого сначала повторим уже изученный материал и выучим формулу для расчёта количества теплоты для плавления и кристаллизации.
2. Итак, начнём с проверки домашнего задания.
Задания для всего класса (на экране) на 5 минут в тетрадях:
I. Пользуясь таблицей «Температура плавления некоторых веществ», отметить на температурной шкале температуры плавления водорода, ртути, льда, цинка, вольфрама
II. Написать в каком состоянии находятся эти вещества при температурах выше этой и ниже этой.
По графику нагревания и таяния льда и нагревания полученной из него воды ответьте на вопросы:
а) Какой участок графика соответствует таянию снега? (ответ ВС)
б) Сколько времени оно примерно длилось?(ответ 2 мин.)
в) До какой температуры нагрелась вода через 5 мин после начала опыта?(ответ 30 0)
Ребята пока вы работаете у доски необходимо ответить на вопросы домашнего задания
1. Плавление и отвердевание.
Ответит Коля
2. График плавления и отвердевания кристаллических тел ответит Аня.
После ответа учащихся по домашним параграфам §13 и §14 с места проверяются ответы учащихся по своим тетрадям.
3. Итак, по результатам нашего общения, я поняла, что обратили внимание на то, что процесс плавления требует времени. Вещество получает энергию, но температура во время этого процесса не изменяется. Почему? В кристаллах молекулы расположены в строгом порядке, хотя и колеблются около своих положений равновесия. При достижении температуры плавления размах молекул увеличивается и порядок в расположении частиц нарушается
Кристаллическая решетка рушится. На это и расходуется поступающая энергия извне. Поэтому на повышение температуры её просто не хватает. Пока всё вещество не расплавится, температура не повысится. Опыты показали, что для 1 кг различных веществ для плавления необходима различная энергия. Её измерили на опытах и внесли в таблицу «Удельная теплота плавления».(стр 37). Итак λ- физическая величина, показывающая, какая энергия необходима для 1 кг вещества, нагретого до температуры плавления, чтобы расплавиться
Она измеряется в Дж/кг
Если необходимо расплавить другую массу, то Q пл =λm
При кристаллизации температура также не изменяется, т.к. вещество отдаёт то же количество теплоты, что получило при плавлении. Поэтому λ можно назвать и удельной теплотой кристаллизации. Q крист = -λm
4. Ребята, откройте таблицу на стр 57.Ответы на вопросы:
а) В каком порядке расположены вещества (Ответ: В порядке убывания удельной теплоты плавления)
б)Что обозначает число 3,9 ·10 5 стоящего против слова алюминий (ответ: Количество теплоты, необходимое 1кг алюминия, чтобы его расплавить)
в) На плавление какого из кубиков медного или алюминиевого пойдёт меньше энергии и во сколько раз, если массы их равны и взяты при температуре плавления?(ответ: медного в 2 раза)
г) Известно, что на плавление куска меди при температуре плавления израсходовано 6,3 · 10 5 Дж энергии. Какое количество теплоты выделится при отвердевании жидкой меди этой массы (ответ: 3 кг; 6,3 · 10 5 Дж)
На воду в теплоизолированных сосудах опущены кусочки льда. В каком из них лёд таять не будет? (Ответ: №3)
Решаем на доске
а) Подчеркнуть одной чертой, что известно в задаче, и записать в дано:
б) Составить блок - схему решения задачи

5. Подводятся итоги сделанного на уроке
6. Домашнее задание: §15, упр. 8(4,5)
Учитель:Сафронова О.А.
Класс:8
Тема урока: « Расчет к оличества теплоты, необходимого для нагревания тела или выделяемого им при охлаждении»
Тип урока: комбинированный.
Форма урока : закрепление знаний, урок - решения задач.
Методы: Метод CASE STUDY способствует развитию различных практических навыков. «Они могут быть описаны одной фразой – творческое решение проблемы и формирование умения анализа ситуации и принятия решения». Словесные, эмоциональные методы; оценка практической значимости содержания обучения, прогнозирование будущей деятельности; логические методы
Средства обучения:
Идеальные средства: устная речь (беседа и т. п.)
Материальные средства обучения – это физические объекты, которые используют учитель и ученик для детализированного обучения
1.Печатные пособия: учебник, таблицы
2.Проекционный материал: слайды,
Цели:
закрепить у учащихся знания по теме: «количество теплоты», «удельная теплоемкость»;
вывести формулу для расчета количества теплоты для различного рода веществ;
обосновать величины, от которых зависит количество теплоты;
определить способы расчета количества теплоты при теплообмене тел;
продолжить формирование навыков критического мышления через организацию учебного диалога и применение знаний классической физики в новой ситуации.
Развивающие:
овладению умениями решать количественные задачи, применять полученные знания для решения физических задач;
использовать приобретенные знания и умения в практической деятельности и повседневной жизни;
содействовать совершенствованию мыслительных операций (анализ, вывод, обобщение);
развитие познавательного интереса учащихся.
развитию эмоциональной сферы, коммуникативной культуры;
содействовать воспитанию средствами урока уверенности в своих силах, в необходимости разумного использования достижений науки и технологий для дальнейшего развития человеческого общества;
формирование умений наблюдать, делать выводы, выделять главное;
развитие памяти, логики, мышления, внимания.
Воспитательные:
формирование научного мировоззрения;
воспитание устойчивого интереса к предмету положительного отношения к знаниям.
Основное содержание урока.
1. Организация обучающихся на работу(организационный момент)
2 .Организация мотивации, постановки учебной задачи, цели Актуализация знаний
3.Планирование предстоящей деятельности
4. Решение задач.
5. Закрепление изученного материала.
6. Оценивание продвижения к цели, рефлексивный анализ деятельности.
2 .Организация мотивации, постановки учебной задачи, цели. Актуализация знаний
Без тепла нет жизни. Но слишком сильный холод и жара разрушает всё живое.
Все тела, даже глыбы льда, излучают энергию, но слабо нагретые тела излучают мало энергии, и это излучение не воспринимается человеческим глазом.
В восемнадцатом веке многие учёные считали, что теплота – это особое вещество «теплород», невесомая «жидкость», содержащаяся в телах. Сейчас мы знаем. Что это не так. Сегодня мы будем говорить о теплоте и тепловых явлениях, а также научимся расчитывать количество теплоты, необходимое для нагревания тела и выделяющееся при его охлаждении
Качественная задача:
Из русской сказки “Лисичка - сестричка и серый волк”. Волк пошел на реку, опустил хвост в прорубь и начал приговаривать: “ Ловись, рыбка, и мала и велика! Ловись, рыбка и мала и велика!”. Вслед за ним и лиса явилась; ходит около волка да причитывает: “ Ясни, ясни на небе звезды! Мерзни, мерзни волчий хвост!”. Хвост и примерз. Каким путем покинуло тепло хвост волка?
Из алтайской сказки “ Горностай и заяц”. Молча думал свою думу мудрый медведь. Перед ним жарко трещал большой костер, над огнем на железном треножнике стоял золотой котел с семью бронзовыми ушками. Этот свой любимый котел медведь никогда не чистил: боялся, что вместе с грязью счастье уйдет, и золотой котел был всегда ста слоями сажи как бархатом покрыт. Влияло ли на нагревание воды то, что котел был покрыт “ ста слоями сажи”?
На предыдущем уроке, мы выяснили, что для нагревания 1 кг вещества на 1ºС требуется количество теплоты, численно равное значению удельной теплоемкости.
Вопрос №1:
Кто мне скажет, что означает: удельная теплоемкость алюминия с=920 Дж/кг*ºС?
Ответ:
Учащиеся дают правильный ответ: для нагревания 1 кг алюминия на 1 ºС, необходимо количество теплоты Q =920 Дж.
Вопрос №2:
Повторим, от каких величин зависит количество теплоты?
На слайдах представлены рисунки, с помощью которых ребята дают подробное объяснение предыдущей темы.
сосуд №1 сосуд №2

m 1
m 2
Ответ:
Количество теплоты зависит от массы тела:
Из рисунка хорошо видно, что масса воды во втором сосуде больше в два раза массы воды в первом сосуде m 2 > m 1 ,следовательно, и количество теплоты Q , которое необходимо, чтобы нагреть эти жидкости, для второго сосуда понадобится и затратится больше.
2. сосуд №1 сосуд №2
m 1
m 2
Q 2 > Q 1
Следовательно, можно сделать вывод о том, что количество теплоты прямо пропорциональна массе вещества: Q m
3. чайник №1 чайник №2


до Т=50ºС до Т=100ºС
Ответ:
Количество теплоты зависит от разности температур :
Чем больше разность температур, тем больше количество энергии нужно затратить. На нагрев чайника №2 затратится больше энергии, чем на нагрев чайника под номером 1.
Следовательно, можно сделать вывод о том, что количество теплоты прямо пропорциональна разности температур: Q Т
4. сосуд №1 сосуд №2

В один сосуд налита вода, в другой – подсолнечное масло.
Какой из сосудов, мы будем дольше нагревать?
Ответ:
На нагревание сосуда с водой мы затратим больше энергии, соответственно, количество теплоты выделиться больше. Так как, удельная теплоемкость воды 4200 Дж/кг*ºС, а удельная теплоемкость масла 1700 Дж/кг*ºС. Поэтому на нагревание воды, мы затратим больше времени, но и остывать вода будет дольше, чем масло, в связи с большим значением теплоемкости.
Вывод: количество теплоты зависит от рода вещества, т.е., от величины удельной теплоемкости: Q с
4. Решение задач. На практике часто пользуются тепловыми расчётами. Например, при строительстве зданий необходимо учитывать, какое количество теплоты должна отдавать зданию вся система отопления. Следует также знать, какое количество теплоты будет уходить в окружающее пространство через окна, стены, двери.
Покажем на примерах, как нужно вести простейшие расчёты.
Чтобы рассчитать количество теплоты, необходимое для нагревания тела или выделяемое им при охлаждении, следует удельную теплоёмкость умножить на массу тела и на разность между конечной и начальной температурами.
Если обозначить массу m, разность между конечной (t 2 ) и начальной (t 1 ) температурами - t 2 - t 1 получим формулу для расчёта количества теплоты:
Q = cm(t 2 - t 1 ).
Задача №1:
Определить, какое количество теплоты необходимо сообщить куску свинца массой 2 кг для его нагревание на 10°С.
Дано: СИ Решение:
m =2 кг по таблице находим для свинца:
с=140 Дж/(кг°С) с=140 Дж/(кг°С)
Δ t=10 °С формула для расчета количества теплоты:
Q =с mΔT
Q -? Подставляем численное значение, получаем:
Q = 140 Дж/(кг °С)*2 кг*10°С=2800 Дж.
Ответ: Q =2800 Дж.
Задача №2:
Какое количество теплоты отдает 5 л воды при охлаждении с 50°С до
10°С?
СИРешение:
V = 5л
с = 4200 Дж/(кг °С)
t 0 = 50°С
t 1 = 10°С
p = 1000 кг/м 3
Так как плотность воды p = 1000 кг/м 3 ,
то масса воды равна:
m = pV
m = 1000 кг/м 3 ·5·10 -3 м 3 =5 кг.
Q = cm ( t 1 - t 0 )
Q = 4200 Дж/(кг °С) ·5 кг·(10°С-50°С) =-=840кДж
Ответ: Q =-840кДж
Q= ?
Знак «-» в ответе указывает на то, что вода отдает тепло.
Для более сильных учеников, учитель предлагает следующую задачу.
Задача №3
Для нагревания куска цинка массой 100 г потребовалось 15 кДж теплоты. До какой температуры был нагрет кусок цинка, если его начальная температура была равна 25°С?
СИРешение:
m =100 г
Q =15 кДж
t 0 = 25°С
с ц = 400 Дж/(кг °С)
0,1 кг
15000 Дж
Температуру, до которой был нагрет кусок цинка определим из формулы расчета количества теплоты:
Q = cm ( t - t 0 )
где
с - удельная теплоемкость цинка
с ц =400 Дж/(кг °С)
вывод формулы:
Q = cm ( t - t 0 )
Q = cmt - cmt 0
с mt = Q + cmt 0
t = ( Q + cmt 0 )/ cm
t = Q / cm + t 0
подставляя числа, вычисляем математически:
t = 15000Дж/400 Дж/(кг °С)*0,1 кг+25°С=400°С
Ответ: t =400°С
t = ?
Задача №4
В железный котёл массой 5 кг налита вода массой 10 кг. Какое количество теплоты нужно передать котлу с водой для изменения их температуры от 10 до 100 °С?
При решении задачи нужно учесть, что оба тела - и котёл, и вода - будут нагреваться вместе. Между ними происходит теплообмен. Их температуры можно считать одинаковыми, т. е. температура котла и воды изменяется на 100 °С - 10 °С = 90 °С. Но количества теплоты, полученные котлом и водой, не будут одинаковыми. Ведь их массы и удельные теплоёмкости различны.
Нагревание воды в котелке

Задача №5
Смешали воду массой 0,8 кг, имеющую температуру 25 °С, и воду при температуре 100 °С массой 0,2 кг. Температуру полученной смеси измерили, и она оказалась равной 40 °С. Вычислите, какое количество теплоты отдала горячая вода при остывании и получила холодная вода при нагревании. Сравните эти количества теплоты.
Запишем условие задачи и решим её.

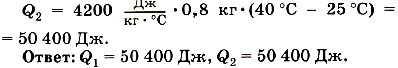
Мы видим, что количество теплоты, отданное горячей водой, и количество теплоты, полученное холодной водой,равны между собой. Это не случайный результат. Опыт показывает, что если между телами происходит теплообмен, то внутренняя энергия всех нагревающихся тел увеличивается на столько, на сколько уменьшается внутренняя энергия остывающих тел.
При проведении опытов обычно получается, что отданная горячей водой энергия больше энергии, полученной холодной водой. Это объясняется тем, что часть энергии передаётся окружающему воздуху, а часть энергии - сосуду, в котором смешивали воду. Равенство отданной и полученной энергий будет тем точнее, чем меньше потерь энергии допускается в опыте. Если подсчитать и учесть эти потери, то равенство будет точным.
7. Информация о домашнем задании, инструктаж по его выполнению.
Какое количество теплоты требуется для нагревания воды массой 0,1 кг на 1 °С?
Рассчитайте количество теплоты, необходимое для нагревания: а) чугунного утюга массой 1,5 кг для изменения его температуры на 200 °С; б) алюминиевой ложки массой 50 г от 20 до 90 °С; в) кирпичного камина массой 2 т от 10 до 40 °С.
Какое количество теплоты выделилось при остывании воды, объём которой 20 л, если температура изменилась от 100 до 50 °С?
Теплоемкость - это количество теплоты, поглощаемой телом при нагревании на 1 градус.
Теплоемкость тела обозначается заглавной латинской буквой С .
От чего зависит теплоемкость тела? Прежде всего, от его массы. Ясно, что для нагрева, например, 1 килограмма воды потребуется больше тепла, чем для нагрева 200 граммов.
А от рода вещества? Проделаем опыт. Возьмем два одинаковых сосуда и, налив в один из них воду массой 400 г, а в другой - растительное масло массой 400 г, начнем их нагревать с помощью одинаковых горелок. Наблюдая за показаниями термометров, мы увидим, что масло нагревается быстрое. Чтобы нагреть воду и масло до одной и той же температуры, воду следует нагревать дольше. Но чем дольше мы нагреваем воду, тем большее количество теплоты она получает от горелки.
Таким образом, для нагревания одной и той же массы разных веществ до одинаковой температуры требуется разное количество теплоты. Количество теплоты, необходимое для нагревания тела и, следовательно, его теплоемкость зависят от рода вещества, из которого состоит это тело.
Так, например, чтобы увеличить на 1°С температуру воды массой 1 кг, требуется количество теплоты, равное 4200 Дж, а для нагревания на 1 °С такой же массы подсолнечного масла необходимо количество теплоты, равное 1700 Дж.
Физическая величина, показывающая, какое количество теплоты требуется для нагревания 1 кг вещества на 1 ºС, называется удельной теплоемкостью этого вещества.
У каждого вещества своя удельная теплоемкость, которая обозначается латинской буквой с и измеряется в джоулях на килограмм-градус (Дж/(кг ·°С)).
Удельная теплоемкость одного и того же вещества в разных агрегатных состояниях (твердом, жидком и газообразном) различна. Например, удельная теплоемкость воды равна 4200 Дж/(кг · ºС), а удельная теплоемкость льда 2100 Дж/(кг · °С); алюминий в твердом состоянии имеет удельную теплоемкость, равную 920 Дж/(кг - °С), а в жидком - 1080 Дж/(кг - °С).
Заметим, что вода имеет очень большую удельную теплоемкость. Поэтому вода в морях и океанах, нагреваясь летом, поглощает из воздуха большое количество тепла. Благодаря этому в тех местах, которые расположены вблизи больших водоемов, лето не бывает таким жарким, как в местах, удаленных от воды.
Расчет количества теплоты, необходимого для нагревания тела или выделяемого им при охлаждении.
Из вышеизложенного ясно, что количество теплоты, необходимое для нагревания тела, зависит от рода вещества, из которого состоит тело (т. е. его удельной теплоемкости), и от массы тела. Ясно также, что количество теплоты зависит от того, на сколько градусов мы собираемся увеличить температуру тела.
Итак, чтобы определить количество теплоты, необходимое для нагревания тела или выделяемое им при охлаждении, нужно удельную теплоемкость тела умножить на его массу и на разность между его конечной и начальной температурами:
Q = cm (t 2 -t 1) ,
гдеQ - количество теплоты, c - удельная теплоемкость, m - масса тела, t 1 - начальная температура, t 2 - конечная температура.
При нагревании тела t 2 > t 1 и, следовательно, Q >0 . При охлаждении тела t 2и < t 1 и, следовательно, Q < 0 .
В случае, если известна теплоемкость всего тела С , Q определяется по формуле: Q = C (t 2 - t 1).
22) Плавление: определение, расчет количества теплоты на плавление или отвердевание, удельная теплота плавления, график зависимости t 0 (Q).
Термодинамика
Раздел молекулярной физики, который изучает передачу энергии, закономерности превращения одних видов энергии в другие. В отличие от молекулярно-кинетической теории, в термодинамике не учитывается внутреннее строение веществ и микропараметры.
Термодинамическая система
Это совокупность тел, которые обмениваются энергией (в форме работы или теплоты) друг с другом или с окружающей средой. Например, вода в чайнике остывает, происходит обмен теплотой воды с чайником и чайника с окружающей средой. Цилиндр с газом под поршнем: поршень выполняет работу, в результате чего, газ получает энергию, и изменяются его макропараметры.
Количество теплоты
Это энергия , которую получает или отдает система в процессе теплообмена. Обозначается символом Q, измеряется, как любая энергия, в Джоулях.
В результате различных процессов теплообмена энергия, которая передается, определяется по-своему.
Нагревание и охлаждение
Этот процесс характеризуется изменением температуры системы. Количество теплоты определяется по формуле
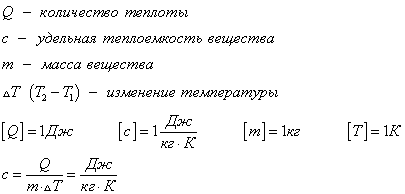
Удельная теплоемкость вещества с измеряется количеством теплоты, которое необходимо для нагревания единицы массы данного вещества на 1К. Для нагревания 1кг стекла или 1кг воды требуется различное количество энергии. Удельная теплоемкость - известная, уже вычисленная для всех веществ величина, значение смотреть в физических таблицах.
Теплоемкость вещества С - это количество теплоты, которое необходимо для нагревания тела без учета его массы на 1К.
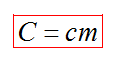
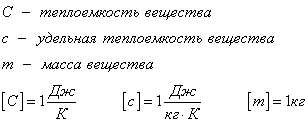
Плавление и кристаллизация
Плавление - переход вещества из твердого состояния в жидкое. Обратный переход называется кристаллизацией.
Энергия, которая тратится на разрушение кристаллической решетки вещества, определяется по формуле

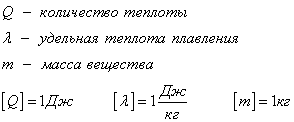
Удельная теплота плавления известная для каждого вещества величина, значение смотреть в физических таблицах.
Парообразование (испарение или кипение) и конденсация
Парообразование - это переход вещества из жидкого (твердого) состояния в газообразное. Обратный процесс называется конденсацией.
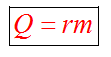

Удельная теплота парообразования известная для каждого вещества величина, значение смотреть в физических таблицах.
Горение
Количество теплоты, которое выделяется при сгорании вещества


Удельная теплота сгорания известная для каждого вещества величина, значение смотреть в физических таблицах.
Для замкнутой и адиабатически изолированной системы тел выполняется уравнение теплового баланса. Алгебраическая сумма количеств теплоты, отданных и полученных всеми телами, участвующим в теплообмене, равна нулю:
Q 1 +Q 2 +...+Q n =0
23) Строение жидкостей. Поверхностный слой. Сила поверхностного натяжения: примеры проявления, расчет, коэффициент поверхностного натяжения.
Время от времени любая молекула может переместиться в соседнее вакантное место. Такие перескоки в жидкостях происходят довольно часто; поэтому молекулы не привязаны к определенным центрам, как в кристаллах, и могут перемещаться по всему объему жидкости. Этим объясняется текучесть жидкостей. Из-за сильного взаимодействия между близко расположенными молекулами они могут образовывать локальные (неустойчивые) упорядоченные группы, содержащие несколько молекул. Это явление называется ближним порядком (рис. 3.5.1).
Коэффициент β называют температурным коэффициентом объемного расширения . Этот коэффициент у жидкостей в десятки раз больше, чем у твердых тел. У воды, например, при температуре 20 °С β в ≈ 2·10 – 4 К – 1 , у стали β ст ≈ 3,6·10 – 5 К – 1 , у кварцевого стекла β кв ≈ 9·10 – 6 К – 1 .
Тепловое расширение воды имеет интересную и важную для жизни на Земле аномалию. При температуре ниже 4 °С вода расширяется при понижении температуры (β < 0). Максимум плотности ρ в = 10 3 кг/м 3 вода имеет при температуре 4 °С.
При замерзании вода расширяется, поэтому лед остается плавать на поверхности замерзающего водоема. Температура замерзающей воды подо льдом равна 0 °С. В более плотных слоях воды у дна водоема температура оказывается порядка 4 °С. Благодаря этому жизнь может существовать в воде замерзающих водоемов.
Наиболее интересной особенностью жидкостей является наличие свободной поверхности . Жидкость, в отличие от газов, не заполняет весь объем сосуда, в который она налита. Между жидкостью и газом (или паром) образуется граница раздела, которая находится в особых условиях по сравнению с остальной массой жидкости.. Следует иметь ввиду, что вследствие крайне низкой сжимаемости наличие более плотно упакованного поверхностного слоя не приводит к сколь-нибудь заметному изменению объема жидкости. Если молекула переместится с поверхности внутрь жидкости, силы межмолекулярного взаимодействия совершат положительную работу. Наоборот, чтобы вытащить некоторое количество молекул из глубины жидкости на поверхность (т. е. увеличить площадь поверхности жидкости), внешние силы должны совершить положительную работу ΔA внеш, пропорциональную изменению ΔS площади поверхности:
Из механики известно, что равновесным состояниям системы соответствует минимальное значение ее потенциальной энергии. Отсюда следует, что свободная поверхность жидкости стремится сократить свою площадь. По этой причине свободная капля жидкости принимает шарообразную форму. Жидкость ведет себя так, как будто по касательной к ее поверхности действуют силы, сокращающие (стягивающие) эту поверхность. Эти силы называются силами поверхностного натяжения .
Наличие сил поверхностного натяжения делает поверхность жидкости похожей на упругую растянутую пленку, с той только разницей, что упругие силы в пленке зависят от площади ее поверхности (т. е. от того, как пленка деформирована), а силы поверхностного натяжения не зависят от площади поверхности жидкости.
Некоторые жидкости, как, например, мыльная вода, обладают способностью образовывать тонкие пленки. Всем хорошо известные мыльные пузыри имеют правильную сферическую форму – в этом тоже проявляется действие сил поверхностного натяжения. Если в мыльный раствор опустить проволочную рамку, одна из сторон которой подвижна, то вся она затянется пленкой жидкости (рис. 3.5.3).
Силы поверхностного натяжения стремятся сократить поверхность пленки. Для равновесия подвижной стороны рамки к ней нужно приложить внешнюю силу Если под действием силы перекладина переместится на Δx , то будет произведена работа ΔA вн = F вн Δx = ΔE p = σΔS , где ΔS = 2L Δx – приращение площади поверхности обеих сторон мыльной пленки. Так как модули сил и одинаковы, можно записать:
|
Таким образом, коэффициент поверхностного натяжения σ может быть определен как модуль силы поверхностного натяжения, действующей на единицу длины линии, ограничивающей поверхность .
Из-за действия сил поверхностного натяжения в каплях жидкости и внутри мыльных пузырей возникает избыточное давление Δp . Если мысленно разрезать сферическую каплю радиуса R на две половинки, то каждая из них должна находиться в равновесии под действием сил поверхностного натяжения, приложенных к границе разреза длиной 2πR и сил избыточного давления, действующих на площадь πR 2 сечения (рис. 3.5.4). Условие равновесия записывается в виде
Если эти силы больше сил взаимодействия между молекулами самой жидкости, то жидкость смачивает поверхность твердого тела. В этом случае жидкость подходит к поверхности твердого тела под некоторым острым углом θ, характерным для данной пары жидкость – твердое тело. Угол θ называется краевым углом . Если силы взаимодействия между молекулами жидкости превосходят силы их взаимодействия с молекулами твердого тела, то краевой угол θ оказывается тупым (рис. 3.5.5). В этом случае говорят, что жидкость не смачивает поверхность твердого тела. При полном смачивании θ = 0, при полном несмачивании θ = 180°.
Капиллярными явлениями называют подъем или опускание жидкости в трубках малого диаметра – капиллярах . Смачивающие жидкости поднимаются по капиллярам, несмачивающие – опускаются.
На рис. 3.5.6 изображена капиллярная трубка некоторого радиуса r , опущенная нижним концом в смачивающую жидкость плотности ρ. Верхний конец капилляра открыт. Подъем жидкости в капилляре продолжается до тех пор, пока сила тяжести действующая на столб жидкости в капилляре, не станет равной по модулю результирующей F н сил поверхностного натяжения, действующих вдоль границы соприкосновения жидкости с поверхностью капилляра: F т = F н, где F т = mg = ρh πr 2 g , F н = σ2πr cos θ.
Отсюда следует:
При полном несмачивании θ = 180°, cos θ = –1 и, следовательно, h < 0. Уровень несмачивающей жидкости в капилляре опускается ниже уровня жидкости в сосуде, в которую опущен капилляр.
Вода практически полностью смачивает чистую поверхность стекла. Наоборот, ртуть полностью не смачивает стеклянную поверхность. Поэтому уровень ртути в стеклянном капилляре опускается ниже уровня в сосуде.
24) Парообразование: определение, виды (испарение, кипение), расчет количества теплоты на парообразование и конденсацию, удельная теплота парообразования.
Испарение и конденсация. Объяснение явления испарения на основе представлений о молекулярном строении вещества. Удельная теплота парообразования. Ее единицы.
Явление превращения жидкости в пар называется парообразованием.
Испарение -процесс парообразования, происходящий с открытой поверхности.
Молекулы жидкости движутся с разными скоростями. Если какая-нибудь молекула окажется у поверхности жидкости, она может преодолеть притяжение соседних молекул и вылететь из жидкости. Вылетевшие молекулы образуют пар. У оставшихся молекул жидкости при соударении меняются скорости. Некоторые молекулы при этом приобретают скорость, достаточную для того, чтобы вылететь из жидкости. Этот процесс продолжается, поэтому жидкости испаряются медленно.
*Скорость испарения зависит от рода жидкости. Быстрее испаряются те жидкости, у которых молекул притягиваются с меньшей силой..
*Испарение может происходить при любой температуре. Но при высоких температурах испарение происходит быстрее.
*Скорость испарения зависит от площади ее поверхности.
*При ветре (потоке воздуха) испарение происходит быстрее.
При испарении внутренняя энергия уменьшается, т.к. при испарении жидкость покидают быстрые молекулы, следовательно, средняя скорость остальных молекул уменьшается. Значит, что если нет притока энергии из вне, то температура жидкости уменьшается.
 Явление превращения пара в жидкость называется конденсацией.
Она сопровождается выделением энергии.
Явление превращения пара в жидкость называется конденсацией.
Она сопровождается выделением энергии.
Конденсацией пара объясняется образование облаков. Пары воды, поднимающиеся над землей, образуют в верхних холодных слоях воздуха облака, которые состоят из мельчайших капель воды.
Удельная теплота парообразования – физ. величина, показывающая какое кол-во теплоты необходимо, чтобы обратить жидкость массой 1 кг в пар без изменения температуры.
Уд. теплоту парообразования обозначают буквой L и измеряется в Дж/кг
Уд. теплоту парообразования воды:L=2,3×10 6 Дж/кг, спирт L=0,9×10 6
Кол-во теплоты, необходимое для превращения жидкости в пар: Q = Lm
